ผิวกระดูกอ่อนข้อเท้าบาดเจ็บ
Management of Osteochondral Lesion of Talar Dome
Management of Osteochondral Lesion of Talar Dome
นพ พิสิฏฐ์ บุญมา
นพ ชำนาญนิติ์ รุ้งพราย
กองออร์โธปืดิกส์
รพ.พระมงกุฎเกล้า
การรักษาภาวะกระดูกอ่อนของเทลัส (Talus)
บาดเจ็บ
ภาวะกระดูกอ่อนของเทลัสบาดเจ็บ (Osteochondral
Lesion of Talus (OLT)) เป็นภาวะที่พบได้บ่อยหลังจากมีการบาดเจ็บของข้อเท้า
ไม่ว่าจะเป็นข้อเท้าพลิก หรือกระดูกข้อเท้าหัก โดยในอดีตมีชื่อเรียกที่ต่าง ๆ กันออกไปตามแต่การสันนิษฐานถึงพยาธิกลไกการเกิดโรค
คือ Osteochondritis Dissecans, Talar Dome Fracture, Transchondral
Fracture และ Flake Fracture การวินิจฉัยโรคมักจำเป็นต้องใช้การส่งตรวจภาพทางรังสีพิเศษ
เช่นการส่งตรวจเอกซเรย์คอมพิวเตอร์ (Computer Topography (CT scan)) หรือ การส่งตรวจด้วยเอกซเรย์คลื่นแม่เหล็กไฟฟ้า (Magnetic
Resonance Imaging (MRI)) ซึ่งการรักษาขั้นต้นคือการรักษาด้วยวิธีการไม่ผ่าตัด
ซึ่งเมื่อการรักษาดังกล่าวล้มเหลวการรักษาโดยการผ่าตัดจึงเข้ามาเป็นส่วนประกอบสำคัญในการรักษา
ความชุกของโรค
มีข้อมูลแตกต่างกันตามแต่ละงานวิจัย
โดยงานวิจัยของ Bosein และคณะ พบว่าโรคกระดูกอ่อนเทลัสบาดเจ็บมีความชุกร้อยละ
4 ในกลุ่มนักศึกษามหาวิทยาลัยจำนวน 121
คนที่มีอาการบาดเจ็บจากข้อเท้าพลิกและได้ทำการถ่ายภาพรังสีเอกซเรย์ โดยมีอีกหลายๆ การศึกษาพบว่าสามารถพบโรคกระดูกอ่อนเทลัสบาดเจ็บในข้อเท้าทั้งสองข้างได้ถึงร้อยละ
10 ซึ่งถ้าศึกษาในกลุ่มผู้ป่วยที่มีภาวะปวดข้อเท้าเรื้อรังจะพบความชุกของโรคเพิ่มสูงมากขึ้น
โดยในกลุ่มผู้ป่วยนี้พบว่าโรคกระดูกอ่อนเทลัสบาดเจ็บเป็นสาเหตุถึง 81%
กลไกการบาดเจ็บ
ข้อเท้าพลิกและภาวการณ์บาดเจ็บจาการบิดหมุนของข้อเท้ามีความเกี่ยวข้อง
และมีรายงานว่าเป็นกลไกที่ทำให้เกิดโรคกระดูกอ่อนเทลัสบาดเจ็บ ซึ่งในอดีตทฤษฎีแรกๆที่อธิบายรอยโรคนี้ในปี
ค.ศ.1922 คือ การเกิดกระดูกอ่อนบาดเจ็บขึ้นมาเอง และในปี ค.ศ. 1959 Bernt
และ Hardy ได้ตั้งทฤษฎีว่าเกิดจากสาเหตุอุบัติเหตุซึ่งเป็นที่นิยมใช้กัน
โดยในปี ค.ศ. 1966 Campbell และ Ranawat ได้นำทั้งสองทฤษฎีมาร่วมกันโดยเกิดจากกลไลภาวะการขาดเลือดและกระดูกหัก
ตำแหน่งของรอยโรค
มีหลายงานวิจัยรายงานว่าตำแหน่งรอยโรคกระดูกอ่อนเทลัสบาดเจ็บพบที่ฝั่งด้านใน
(Medial)
มากกว่าฝั่งด้านนอก (Lateral) Canale รายงานว่ารอยโรคด้านในเกิดจากอุบัติเหตุประมาณ
64% ซึ่งต่างจากรอยโรคด้านนอกที่พบว่ามีประวัติอุบัติเหตุเกิดขึ้นทั้งหมด
โดยรอยโรคด้านในมักจะลึกและกลายเป็นถุงน้ำ ในขณะที่รอบโรคด้านนอกมักจะตื้น
เป็นแผ่นบางๆ (Wafer/Flake) โดยการศึกษาปัจจุบันพบว่าโรคกระดูกอ่อนเทลัสบาดเจ็บ
53% อยู่ในตำแหน่งด้านในบริเวณส่วนกลางของข้อเท้า และ 26%
อยู่ในตำแหน่งด้านนอกและตรงกลางของข้อเท้า ซึ่งเมื่อมาดูว่าโรคกระดูกอ่อนเทลัสบาดเจ็บส่วนใหญ่จะอยู่ตรงส่วนกลางของข้อเท้าถึงร้อยละ
80 โดยมีอยู่ส่วนหน้า และส่วนหลังของข้อเท้าเป็น 6% และ 14%
ตามลำดับ
ประวัติและการตรวจร่างกาย
ผู้ป่วยมักมาด้วยอาการปวด
บวม ข้อเท้าติด หรือในบางรายมาด้วยอาการข้อเท้าล๊อค
ผู้ป่วยมักให้ประวัติการบาดเจ็บที่ข้อเท้า รวมถึงอาจมีภาวะข้อเท้าไม่มั่นคงร่วมด้วย
การตรวจร่างกายพบจุดกดเจ็บ พิสัยของข้อลดลง เจ็บขณะทำการพลิกข้อเท้าเข้าในและกระดกข้อเท้า
อาจร่วมกับภาวะข้อเท้าบวม
ซึ่งแม้ว่าตรวจร่างกายจะไม่พบอาการแสดงดังที่ได้กล่าวไปก็ไม่สามารถวินิจฉัยแยกโรคกระดูกอ่อนเทลัสบาดเจ็บออกได้
ซึ่งมักจำเป็นต้องใช้การส่งตรวจภาพถ่ายทางรังสีเพื่อช่วยในการวินิจฉัย
การตรวจทางรังสีวิทยา
ภาพถ่ายเอกซเรย์มักเป็นการส่งตรวจลำดับแรกๆในการประเมินอาการทางข้อเท้า
ในอดีตการส่งเอกซเรย์เป็นวิธีที่ใช้ในการวินิจฉัยโรคกระดูกอ่อนเทลัสบาดเจ็บ โดยปีค.ศ.
1947 Ray
และ Coughlin แนะนำให้ส่ง Oblique Film
ร่วมกันการส่งภาพ AP และ Lateral เพื่อให้กระดูกเทลัสไม่โดนขวางด้วยกระดูกตาตุ่มทั้ง 2 ข้าง
ซึ่งในภาพหลังเรียกภาพถ่ายทางรังสีดังกล่าวว่า Mortise View ร่วมกับการกดข้อเท้าลงให้มากที่สุด
เพื่อให้เห็นรอบโรคบริเวณด้านหลังของกระดูกเทลัส อย่างไรก็ตามในรายงานของ Verhagen
และคณะพบว่า ผู้ป่วยถึง 41% มีการวินิจฉัยผิดพลาด
ถ้าใช้เพียงแค่ภาพถ่ายทางรังสีในการวินิจฉัย ซึ่งมีงานวิจัยอื่นๆ บอกไปในทางเดียวกัน
อย่างที่ได้กลาวไปการส่งภาพถ่ายทางรังสีเป็นการส่งลำดับแรกๆ ที่ใช้ในการช่วยวินิจฉัยแต่อย่างไรก็ตามมีความไวต่ำ
มักจำเป็นต้องส่งการตรวจทางรังสีอื่นๆ เพื่อช่วยในการวินิฉัยร่วมกับขนาดของรอยโรค
ภาพถ่ายคลื่นแม่เหล็กไฟฟ้า (MRI)
ภาพถ่ายคลื่นแม่เหล็กไฟฟ้า (MRI)
เป็นการส่งภาพถ่ายทางรังสีที่ทำให้รู้จักโรคกระดูกอ่อนเทลัสบาดเจ็บ
ซึ่งพบตั้งแต่ปี ค.ศ.1987 อย่างไรก็ตามในขณะนั้นยังไม่ได้เป็นการส่งตรวจที่แนะนำในการใช้เพื่อวินิจฉัย
โดยภาพถ่ายคลื่นแม่เหล็กไฟฟ้าช่วยให้เห็นรอยโรคในเนื้อเยื่ออ่อนซึ่งทำให้มีประโยชน์ในการประเมินรอยโรคที่กระดูกอ่อน
ซึ่งเมื่อทำการตรวจจะพบ Low intensity ใน T1 และมีสัญญาณเข้มขึ้นบริเวณรอยต่อของรอยโรคในภาพ T2 ซึ่งมีการศึกษาพบว่าภาพถ่ายคลื่นแม่เหล็กไฟฟ้ามีความไวร้อยละ
96 และความจำเพาะถึงร้อยละ 96 นอกจากนี้ยังช่วยประเมินความมั่นคง (Stability)
ของรอยโรคได้อีกด้วย จากที่กล่าวมาการส่งตรวจภาพคลื่นแม่เหล็กไฟฟ้า
ปลอดภัยและมีความแม่นยำสูงในการวินิจฉัยโรค จึงมักใช้ในการส่งตรวจหลังจากภาพถ่ายรังสี
การส่งตรวจเอกซเรย์คอมพิวเตอร์ (CT)
การส่งตรวจเอกซเรย์คอมพิวเตอร์
สามารถดูรอยโรคกระดูกได้ดีกว่าการตรวจโดยคลื่นแม่เหล็กไฟฟ้า โดย Verhagen
และคณะ ทำการศึกษาพบว่า เอกซเรย์คอมพิวเตอร์มีค่าความไวและความจำเพาะต่อโรคกระดูกอ่อนเทลัสบาดเจ็บ
เป็นร้อยละ 81 และ 99 ตามลำดับ เมื่อมาศึกษาทางสถิติพบว่าไม่มีความต่างอย่างมีนัยยะสำคัญทางสถิติกับเอกซเรย์คลื่นแม่เหล็กไฟฟ้า
เอกซเรย์คอมพิวเจอร์นั้นสามารถประเมินความลึกของรอยโรคได้แม่นยำ
อย่างไรก็ตามไม่สามารถประเมินรอยโรคระยะต้นได้เนื่องจากกระดูกอ่อนไม่สามารถเห็นได้จากภาพถ่ายเอกซเรย์คอมพิวเตอร์
ซึ่งการทำเอกซเรย์แบบ Single Photon Emission Computerized Tomography
(SPECT) สามารถช่วยหารอยโรคได้ดียิ่งขึ้น โดย Tammam และคณะ พบว่า SPECT-CT สามารถใช้ประเมินโรคกระดูกอ่อนเทลัสบาดเจ็บได้เทียบเท่าเอกซเรย์คลื่นแม่เหล็กไฟฟ้า
ซึ่งในบางสถาบันแนะนำให้ใช้ SPECT-CT เพื่อประเมินโรคกระดูกอ่อนเทลัสบาดเจ็บ
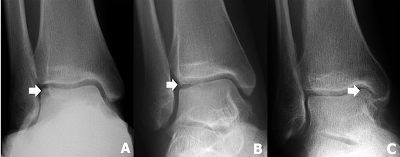
ภาพที่ 1 แสดงภาพถ่ายทางรังสีวิทยาของรอยโรคกระดูกอ่อนเทลัสบาดเจ็บ
(A)
รอยโรคด้านนอก Berndt
และ Harty ระยะที่ 3
(B)
รอยโรคด้านนอก Berndt
และ Harty ระยะที่ 4
(C) รอยโรคด้านใน
Berndt
และ Harty ระยะที่ 2
ระยะของโรค (Staging)
โรคกระดูกอ่อนเทลัสบาดเจ็บได้มีการจัดแบ่งระยะโรคตามลักษณะทางภาพถ่ายรังสีตั้งแต่ปี
ค.ศ.1959 โดย Berndt และ Harty (ตารางที่ 1) ซึ่งการแบ่งระยะโรคดังกล่าวช่วยให้เข้าใจลักษณะของตัวโรคและแนวทางการรักษา
อย่างไรก็ตามในปัจจุบันการจัดแบ่งระยะโรคโดยภาพถ่ายทางรังสีมีความละเอียดไม่เพียงพอ
แต่ยังสามารถนำมาประยุกต์ใช้กับการแบ่งระยะโรคในปัจจุบันได้
ตารางที่ 1
แสดงการแบ่งระยะโรคโรคกระดูกอ่อนเทลัสบาดเจ็บโดยใช้ภาพถ่ายทางรังสี
ระยะโรค
|
ความหมาย
|
I
|
การหักแบบโดนแรงกด โดยผิวกระดูกอ่อนยังคลุมกระดูกทั้งหมด
|
II
|
ชิ้นส่วนกระดูกอ่อนและผิวกระดูกหักแบบมีส่วนที่ติดกับส่วนที่ไม่หักอยู่
|
III
|
ชิ้นส่วนกระดูกอ่อนและผิวกระดูกหัก
แต่ยังไม่เคลื่อน
|
IV
|
ชิ้นส่วนกระดูกอ่อนและผิวกระดูกหัก
และเคลื่อนเข้าไปอยู่ในข้อเท้า
|
ตารางที่ 2
แสดงการแบ่งระยะโรคโรคกระดูกอ่อนเทลัสบาดเจ็บโดยใช้ภาพถ่ายคลื่นแม่เหล็กไฟฟ้า
ระยะโรค
|
ความหมาย
|
0
|
กระดูกอ่อนปกติ
|
I
|
พบสัญญาณผิดปกติที่กระดูกอ่อนแต่กระดูกอ่อนคลุมผิวกระดูกทั้งหมด
|
II
|
กระดูกอ่อนเริ่มเป็นริ้วแต่ผิวกระดูกอ่อนยังคลุมกระดูกทั้งหมด
|
III
|
กระดูกอ่อนหลุดลอกออกเป็นฝา ทำให้ผิวกระดูกสัมผัสกับน้ำในข้อ
|
IV
|
กระดูกอ่อนและผิวกระดูกหัก แต่ยังไม่เคลื่อน
|
V
|
กระดูกอ่อนและผิวกระดูกหัก และเคลื่อนเข้าไปในข้อ
|
มีการแบ่งระยะโรคมากมาย ที่ใช้ภาพถ่ายคลื่นแม่เหล็กไฟฟ้าในการแบ่งระยะโรค
โดยบุคคลแรกที่อธิบายคือ Anderson และคณะ ซึ่งดัดแปลงจาก
Berndt และ Harty โดยเพิ่มระยะโรคที่ 2A
ซึ่งสัมพันธ์กับการมีถุงน้ำใต้ชั้นกระดูกอ่อน Mintz และคณะ พบว่า มีความสัมพันธ์ถึงร้อยละ 83 เมื่อนำภาพถ่ายคลื่นแม่เหล็กไฟฟ้าและจากการส่องกล้องวินิจฉัย
(ตารางที่ 2) และเมื่อจัดกลุ่มใหม่โดยแบ่งเป็น
กลุ่มไม่เป็นโรค(ระยะโรคที่ 0-I) และกลุ่มเป็นโรค(ระยะโรคที่
II-V) พบว่ามีความไวถึง 95% และความจำเพาะถึง
100% โดย Heppel และคณะได้จัดแบ่งระยะโรคโดยใช้ภาพถ่ายคลื่นแม่เหล็กไฟฟ้า
(ตารางที่ 3 และ ภาพที่ 2)
ภาพที่ 2 แสดงภาพถ่ายคลื่นแม่เหล็กไฟฟ้าของรอยโรคกระดูกอ่อนเทลัสบาดเจ็บ
(A) ภาพถ่ายตัดจากหน้าไปหลังของ Hepple ระยะที่ 1
(B) ภาพถ่ายตัดจากหน้าไปหลังของ Hepple ระยะที่ 2A (ลูกศร)
(C,D) ภาพถ่ายตัดจากบนลงล่างของ Hepple ระยะที่ 2A
(E) ภาพถ่ายตัดขวางของ Hepple ระยะที่ 3
(F) ภาพถ่ายตัดขวางของ Hepple ระยะที่ 4
ตารางที่ 3
แสดงการแบ่งระยะโรคโดยใช้ภาพรังสีคลื่นแม่เหล็กไฟฟ้า
ระยะโรค
|
ความหมาย
|
1
|
การบาดเจ็บที่อยู่เฉพาะที่กระดูกอ่อน
|
2a
|
กระดูกอ่อนบาดเจ็บร่วมกับมีกระดูกช้ำและหัก
|
2b
|
กระดูกอ่อนบาดเจ็บ โดยไม่มีภาวะกระดูกช้ำ
|
3
|
กระดูกอ่อนหลุดลอก แต่ไม่เคลื่อน
|
4
|
กระดูกอ่อนหลุด และเคลื่อน
|
5
|
มีภาวะถุงน้ำใต้ชั้นกระดูกอ่อน
|
การจัดแบ่งระยะโรคโดยเอกซเรย์คอมพิวเตอร์ได้เสนอโดย
Ferkel
และคณะ (ตารางที่ 4) ซึ่งคณะนั้นได้ใช้ภาพถ่ายเอกซเรย์คอมพิวเตอร์ในการแบ่งระยะโรค
อย่างไรก็ตามการแบ่งดังกล่าวไม่บ่งบอกถึงพยากรณ์โรค
ตารางที่ 4
แสดงการแบ่งระยะโรคโดยใช้ภาพถ่ายเอกซเรย์คอมพิวเตอร์
ระยะโรค
|
ความหมาย
|
I
|
ถุงน้ำใต้ชั้นกระดูกอ่อนโดยมีผิวกระดูกอ่อนคลุมอยู่
|
IIA
|
ถุงน้ำใต้ชั้นกระดูกอ่อน
โดยมีทางเชื่อมต่อกับผิวข้อ
|
IIB
|
ผิวเปิดบริเวณกระดูกอ่อน
|
III
|
กระดูกอ่อนหลุดแต่ไม่เคลื่อน
|
IV
|
กระดูกอ่อนและหลุดเคลื่อน
|
การแบ่งระยะโรคโดยใช้การส่องกล้องได้เริ่มอธิบายโดย
Pritsch
และคณะในปี ค.ศ. 1986 และทำให้เข้าใจว่ารอยโรคไม่ได้สัมพันธ์กับการแบ่งระยะโรคโดย
Berndt และ Harty หลังจากนั้นได้มีการแบ่งระยะโรคโดย
Ferkel และ Cheng โดยดูลักษณะของกระดูกอ่อนบาดเจ็บซึ่งช่วยในการพยากรณ์โรคของผู้ป่วย
โดยผู้ป่วยที่มีระยะโรค A-C มีแนวโน้มที่จะมีผลการรักษาที่ดีกว่าผู้ป่วยที่มีระยะโรค
D-F เมื่อใช้การประเมินด้วย Modified Weber และ AOFAS (ตารางที่ 5)
ตารางที่ 5
แสดงการแบ่งระยะโรคโดยใช้การส่องกล้อง
ระยะโรค
|
ความหมาย
|
A
|
ผิวกระดูกอ่อนเรียบ ไม่มีรอย แต่นิ่ม
|
B
|
ผิวกระดูกอ่อนขุรขระ
|
C
|
ผิวกระดูกอ่อนเป็นริ้ว
|
D
|
ผิวกระดูกอ่อนเป็นแผ่นลอกและเห็นผิวกระดูก
|
E
|
ผิวกระดูกอ่อนไม่มั่นคงแต่ไม่เคลื่อนหลุด
|
F
|
ผิวกระดูกอ่อนเคลื่อนหลุด
|
การดำเนินโรคของโรคกระดูกอ่อนเทลัสบาดเจ็บยังคงเป็นที่สงสัยเนื่องจากมีความหลากหลายในการศึกษา
มีการรักษามากมายที่ใช้เพื่อการรักษาซึ่งรวมถึงการรักษาโดยการไม่ผ่าตัด (พัก,
ปรับพฤติกรรม, ใส่เฝือก) และการรักษาโดยการผ่าตัด (เอาชิ้นกระดูกอ่อนออก.
เอาชิ้นกระดูกอ่อนร่วมกับขูดผิดกระดูก, เอาชิ้นกระดูกอ่อนออกร่วมกับการใช้กระดูกของผู้ป่วยใส่เพิ่มเข้าไป,
การใช้กระดูกอ่อนเด็ก หรือการใช้กระดูกอ่อนจากผู้บริจาค)
อย่างไรก็ตามยังไม่มีการศึกษาที่แนะนำตามหลักฐานทางวิทยาศาสตร์เพียงพอในปัจจุบัน
การรักษาแบบไม่ผ่าตัด
การรักษาแบบไม่ผ่าตัดเป็นการรักษาลำดับแรก
ในกรณีที่ผู้ป่วยมีรอยโรคกระดูกอ่อนเทลัสบาดเจ็บที่ไม่เคลื่อนหลุด (Berndt
และ Harty I, II, III หรือผิวกระดูกอ่อนไม่มีรอย
โดยวินิจฉัยจากการส่องกล้อง) อย่างไรก็ตามในการศึกษาปัจจุบันไม่ได้ให้ข้อมูลการรักษาแบบไม่ผ่าตัดว่าจะให้ใช้ในช่วง
การบาดเจ็บระยะแรก หรือการบาดเจ็บระยะเรื้อรัง โดยในปัจจุบันที่เป็นที่ยอมรับแล้วคือ
ข้อห้ามในการรักษาแบบไม่ผ่าตัดคือการที่รอยโรคกระดูกอ่อนเทลัสบาดเจ็บหลุดเคลื่อนเข้าไปในข้อ
การรักษาแบบไม่ผ่าตัด มักใช้วิธีการ
พักและจำกัดกิจกรรม การใช่เฝือกและงดการลงน้ำหนัก ซึ่งอาจใช้ยาแก้ปวดร่วมด้วยได้
โดยใช้การรักษาประมาณ 3 สัปดาห์ถึง 4 เดือน จากนนั้นจึงเริ่มด้วยการเดินลงน้ำหนักในรองเท้าบูทที่ควบคุมการขยับของข้อเท้า
และการกายภาพเป็นเวลาต่ออีก 6-10 สัปดาห์
โดยจุดประสงค์ของการรักษาโดยวิธีไม่ผ่าตัดคือลดแรงที่กระทำต่อกระดูกอ่อน
ซึ่งช่วยให้ชิ้นกระดูกอ่อนสามารถติดกลับไปในตำแหน่งเดิมได้ อย่างไรก็ตาม
การรักษาแบบไม่ผ่าตัดยังไม่มีข้อสรุปว่าจะต้องใช้เวลานานเท่าไร, จำกัดการเคลื่อนไหวเท่าไร,
การใช้ยารักษา หรือการกายภาพบำบัด
ผลการรักษาแนวทางการไม่ผ่าตัดของโรคกระดูกอ่อนเทลัสบาดเจ็บมีรายงานที่มีความหลากหลายทั้งวิธีการรักษา
และผลการรักษา การรักษาโดยวิธีการพักและจำกัดกิจกรรมได้ผลดีถึงดีเยี่ยมที่ร้อยละ
59 ในขณะที่รักษาโดยการใช่เฝือกได้ผลดีถึงดีเยี่ยมที่ร้อยละ 41 ซึ่ง Klammer
และคณะพบว่าโรคกระดูกอ่อนเทลัสบาดเจ็บที่มีอาการเพียงเล็กน้อยที่ได้รักษาแบบไม่ผ่าตัดมีร้อยละ
86ที่อาการไม่แย่มากขึ้น (43 ใน 48 ข้อเท้า) และได้มีงานวิจัยล่าสุดที่ทำการรวมข้อมูลวิจัยโดย
Tol และคณะพบว่าการรักษาแบบไม่ผ่าตัดมีผลการรักษาดีถึงดีเยี่ยมที่
45% (91/201 คน) ถึงอย่างไรก็ตาม ความสำเร็จในการรักษาโรคกระดูกอ่อนเทลัสบาดเจ็บยังคงเป็นที่ถกเถียงกันอยู่
นอกจากการศึกษาเรื่องผลการรักษาแล้ว มีรายงานจำนวนหนึ่งพบว่ามีข้อเท้าเสื่อมหลงัจากการรักษาแบบไม่ผ่าตัดถึงร้อยละ
50 นอกจากนี้ยังไม่สามารถบอกได้ว่าการผ่าตัเสามารถช่วยป้องกันการเสื่อมของข้อเท้า โดยมีการศึกษาของ McCullough และคณะพบว่า หลังจากติดตามไป 15 ปี 11 เดือน รอยโรคกระดูกอ่อนเทลัสบาดเจ็บไม่หาย
อย่างไรก็ตามคนไข้ไม่มีอาการปวดและข้อเสื่อมพบได้เพียงเล็กน้อย ซึ่งเป็นการศึกษาติดตามผู้ป่วย
10 คน และยังมีงานวิจัยที่เปรียบเทียบภาพถ่ายทางรังสีระหว่างกลุ่มที่ผ่าตัดและกลุ่มไม่ผ่าตัดพบว่าไม่มีความแตกต่างกัน
ปัจจัยที่สำคัญในการพยากรณ์โรค
มีการศึกษามากมายที่ศึกษาปัจจัยที่มีผลต่อการรักษาโรคกระดูกอ่อนเทลัสบาดเจ็บ
ซึ่งปัจจัยหลักมุ่งไปถึงภาวะของผู้ป่วย และรอยโรคของกระดูกเทลัส
โดยรอยโรคที่ขนาดเล็กกว่า 15 มิลลิเมตร รอยโรคที่มีขอบชัด (Contained
Lesion) และรอยโรคที่อยู่ตำแหน่งส่วนหน้าด้านนอก (Anterolateral)
เป็นปัจจัยที่พบว่าการผ่าตัดจะได้ผลการรักษาที่ดี
โดยปัจจัยที่บ่งบอกว่าการผ่าตัดผลการรักษาจะไม่ค่อยดีได้แก่ อายุมากกว่า 33-40ปี
รอยโรคลึกกว่า 7 มิลลิเมตร รอยโรคใหญ่กว่า 15 มิลลิเมตร มีถุงน้ำเป็นส่วนประกอบ
รอยโรคอยู่ในฝั่งข้อเท้าด้านใน ค่าดัชนีมวลกายสูง (Higher BMI) ประวัติการบาดเจ็บ ระยะเวลาของอาการ และมีภาวะข้อเสื่อม
การรักษาโดยการผ่าตัด
เป้าหมายเพื่อการที่ฟื้นฟูการทำงานของข้อเท้าและลดอาการปวด
โดยการนำกระดูกอ่อนส่วนที่บาดเจ็บออก การทำความสะอาดส่วนที่บาดเจ็บ
และแต่งขอบกระดูกอ่อน รวมถึงการกระตุ้นให้มีการรักษาได้ดีขึ้น การขูด การเจาะ
และการทำไมโครแฟคเจอร์ เป็นหัตถการที่แนะนำให้ทำในกรณีรอยโรคมีขนาดเล็กคือ
เล็กกว่า 15 มิลลิเมตร และลึกน้อยกว่า 7 มิลลิเมตร ในขณะที่รอยโรคขนาดใหญ่หรือล้มเหลวในการรักษาด้วยวิธีการผ่าตัดด้วยวิธีการกระตุ้นไขกระดูก
(Bone
Marrow Stimulation) ควรรักษาด้วยวิธีการนำเซลล์กระดูกอ่อนของผู้ป่วยมาเพาะเลี้ยงและใส่กลับเข้าไป
(Autologous Chondrocyte Implantation; ACI) การส่งถ่ายชื้นส่วนกระดูกอ่อนจากตำแหน่งอื่นของผู้ป่วย
(Osteochondral Autograft Transplantation; OATs/Mosaicplasty) การส่งถ่ายชิ้นส่วนกระดูกอ่อนจากผู้บริจาด (Osteochondral
Allograft Transplantation) หรือการใส่อุปกรณ์โลหะแทนที่ (Metal
Inlay Implant)
ข้อบ่งชี้ในการผ่าตัดคือ
การไม่ประสบความสำเร็จในการรักษาแบบอนุรักษ์นิยม โดยใช้เวลารักษาไม่น้อยกว่า 6
สัปดาห์ ถึง 6 เดือน
ภาวการณ์รักษาโรคกระดูกอ่อนเทลัสบาดเจ็บแบบฉับพลันโดยเป็นระดับ Berndt และ Harty III และ IV อย่างไรก็ตามไม่ได้มีการศึกษาที่บ่งบอกระยะเวลาที่แน่นอนเพื่อนชรักษาด้วยการผ่าตัด
โดย O’Farrell และคณะแนะนำเวลาที่เหมาะสมคืออยู่ในช่วงไม่เกิน
12 เดือนหลังจากการบาดเจ็บ โดย Alexander และคณะ
ได้ติดตามผู้ป่วยที่รักษาในระยะเวลาที่ต่างกัน (ตั้งแต่ 3 ถึง 36 เดือน) พบว่าไม่มีความแตกต่างกันในเรื่องผลการรักษาโดยการผ่าตัด
โดยแผนการดูแลหลังผ่าตัดไม่ได้มีจำเพาะเพียงแต่เน้นไปที่การเริ่มขยับพิสัยของข้อ
ตามด้วยการป้องกันการลงน้ำหนัก และการกลับไปเล่นกีฬา
การจัดท่า
ท่านอนหงายเป็นท่าที่ใช้ในการรักษาไม่ว่าจะเป็นการรักษาผ่าตัดแบบเปิดหรือการรักษาโดยการส่องกล้องที่รอบโรคอยู่ในตำแหน่งส่วนหน้าและส่วนกลางของกระดูกเทลัส
ท่านอนคว่ำใช้ในกรณีการผ่าตัดแบบส่องกล้องกรณีรอยโรคอยู่บริเวณส่วนหลังของกระดูกเทลัส
เทคนิคการผ่าตัด
การผ่าตัดแบบเปิด การรักษาโรคกระดูกอ่อนเทลัสบาดเจ็บบริเวณด้านนอกทั้งส่วนหน้าและส่วนกลางสามารถรักษาได้ด้วยทั้งการผ่าตัดแบบเปิดและวิธีการส่องกล้อง
โดยการผ่าตัดแบบเปิดจะสามารถใช้การลงแผลทั้งแบบเข้าทางด้านหน้าฝั่งนอก (Anterolateral)
ด้านหน้า (Anterior) และการเข้าโดยการตัดกระดูกฟิบิลล่า
หรือ กระโกตาตุ่มด้านนอก (Fibular Osteotomy) ในขณะที่รอยโรคด้านหลังส่วนด้านข้างสามารถเข้าได้ด้วยการส่องกล้องทางด้านหลัง
หรือ การผ่าตัดแบบเปิด โดยลงแผลทางด้านหลังด้านนอก (Posterolateral)
รอยโรคทางด้านหน้าส่วนใน
และส่วนกลางสามารถเข้าถึงโดยใช้การส่องกล้องทางด้านหน้า หรือการผ่าตัดแบบเปิด
โดยสามารถใช้การลงมีดทางด้านหน้า (Anterior) หรือโดยวิธีการตัดกระดูกตาตุ่มใน
(Medial Malleolar Osteotomy) ในขณะที่รอบโรคทางด้านหลังส่วนใน
สามารถเข้าถึงโดยการส่องกล้อง การตัดกระดูกตาตุ่มใน
หรือการผ่าดัดแบบเปิดโดยลงมีดด้านหลังส่วนใน (Posteromedial)
การผ่าตัดแบบส่องกล้อง การส่องกล้องโดยเข้าทางด้านหน้าโดยใช้ช่องทางด้านข้าง และ ด้านใน (Anteromedial; AM and Anterolateral; AL) ร่วมกับที่ดึงข้อเท้า
สามารถใช้ในการรักษาการรักษาโรคกระดูกอ่อนเทลัสบาดเจ็บ ในบางครั้งอาจต้องใช้ช่องเสริมทางด้านหน้าส่วนใน
(Accessory Anteromedial Portal) เพื่อให้สามารถเข้าถงรอยโรคด้านในของข้อเท้าได้
ในขณะเดียวกันการส่องกล้องโดยใช้ช่องทางด้านหลังส่วนในและส่วนนอก
เพื่อจัดการรอยโรคด้านหลังของกระดูกเทลัส โดยที่มีการศึกษาพบว่าการส่องกล้องทางด้านหลังสามารถเข้าไปจัดการกับพื้นที่ได้ถึงร้อยละ
54
วิธีการรักษาด้วยวิธีผ่าตัด
การตัดกระดูกส่วนที่บาดเจ็บออก (Excision)
ชิ้นกระดูกที่หลุดลอยสามารถทำให้เกิดอาการเจ็บในข้อเท้าได้เนื่องจากอาจไปทำให้เกิดการอักเสบ
ขัดขวางพิสัยของข้อ และทำให้กระดูกอ่อนส่วนอื่นบาดเจ็บ โดยมีการศึกษาพบว่าโอกาสสำเร็จในการรักษาวิธีนี้อยู่ที่
33 -92 เปอเซ็นต์
การกระตุ้นไขกระดูก (Bone
Marrow Stimulation)
การตัดกระดูกที่บาดเจ็บออกร่วมกับการขูดผิวกระดูก
ชิ้นส่วนกระดูกอ่อนที่หลุดและขอบกระดูกอ่อนที่ไม่มั่นคงจะสามารถทำการแต่งและขูดได้ทั้งวิธีส่องกล้องและผ่าตัดแบบเปิด
โดยมีงานวิจัยศึกษาพบว่าวิธีนี้มีโอกาสสำเร็จประมาณ 63 เปอร์เซ็นต์ (119
ใน 189คน) อย่างไรก็ตามความสำเร็จในการรักษาอยู่ที่ 47 ถึง 89
เปอร์เซ็นต์จากงานวิจัยทั้งหมด 9 การศึกษา
โดยที่การรักษาผ่าตัดแบบเปิดสำเร็จที่ร้อยละ 57 (28 ใน 49คน)
ในขณะที่การส่องกล้องสำเร็จถึงร้อยละ 65 (91ใน 140 คน)
การตัดกระดูก ขูดกระดูก
ร่วมกับการเจาะผิวกระดูก (Microfracture)
หรือการเจาะด้วยสว่าน
การเจาะผิวกระดูก
(Microfracture) ช่วยเร่งการหายของกระดูกอ่อนด้วย
กระดูกอ่อนแบบ ไฟโบรคาทิเลจ (Fibrocartilage) ซึ่งได้ผลการรักษาที่ดี
โดยรอยโรคด้านหน้าและส่วนกลางของกระดูกเทลัสสามารถรักษาด้วยการส่องกล้องได้ โดยใช้
เหล็กปลายแหลม (Awl/Chondral pick) ที่มีมุมองศาต่าง ๆ
กันเจาะ ซึ่งอาจใช้ร่วมกับช่องเสริมร่วมด้วยได้ โดยการเจาะจะเจาะให้มีระยัห่าง 3-4
มิลลิเมตร กระตุ้นให้เกิดการหลั่งของ สเตมเซลล์ สารกระตุ้นการเจริญเติบโต (Growth
Factors) และโปรตีนที่ช่วยในการรักษา โดยกลไลการแข็งตัวของเลือดจะทำให้เกิดไฟบริน
(Fibrin clot) เพื่อให้เกิดการสร้างกระดูกอ่อนไฟโบรคาทิเลจ
ซึ่งประกอบไปด้วยคอลลาเจนชนิดที่ 1 (Type I Collagen) ซึ่งการทำการเจาะผิวกระดูกสามารถรักษาได้ทั้งภาวะกระดูกอ่อน
หรือภาวะกระดูกร่วมกับกระดูกอ่อนบาดเจ็บ ข้อบ่งชี้คือเป็นการรักษาลำดับต้น
โดยเฉพาะรอบโรคที่มีขนาดเล็กกว่า 1.5 ตารางเซนติเมตร
อย่างไรก็ตามข้อเสียของการรักษาวิธีนี้คือความทนทานของไฟโบรคาทิเลจต่ำกว่าชนิด
ไฮยาลินคาทิเลข (Hyalin Cartilage)
ความสำเร็จของการรักษาภาวะโรคกระดูกอ่อนเทลัสบาดเจ็บมีรายงานในหลายการศึกษา
Beacher และคณะพบว่าผู้ป่วย 45 คนมีอาการดีขึ้น โดย 31 ใน 39
คนมีระดับอยู่ที่ดีถึงดีมากของคะแนน Hannover และอาการปวดดีขึ้น
(คะแนนปวดลดลงจาก 6.5/10 เป็น 2.4/10) โดยมีระยะติดตามเฉลี่ยที่ 5.8ปี Chuckpaiwong
และคณะ ศึกษาคนไข้ 105
คนที่ทำการผ่าตัดส่องกล้องด้านหน้าร่วมกับเจาะผิวกระดูก พบว่ามีคะแนนการทำงานของข้อเท้า
และ อาการปวดดีขึ้น โดยคำนวณจาก VAS และ คะแนน AOFAS (VAS จาก 8.2/10 เป็น 3.8/10 และ AOFAS จาก 42 เป็น 68 หลังจากผ่าตัดได้ 12 เดือน) นอกจากนี้คณะวิจัยยังรายงานถึงการทำเจาะผิวกระดูกซ้ำหลังจากล้มเหลวในการทำครั้งแรก
โดยพบว่ามีคะแนน AOFAS ดีขึ้น 17.2 คะแนน นอกจากนนี้ Kuni
และคณะได้ทำการศึกษาภาพคลื่นแม่เหล็กไฟฟ้าพบว่า ขนาดของรอยโรคเล็กลง
รวมทั้งคะแนน AOFAS หลังผ่าตัดดีขึ้น (ค่าเฉลี่ยที่ 87.5
คะแนน)
โดยล่าสุดมีการศึกษาเปรียบเทียบระหว่าง
การทำกระตุ้นไขกระดูก การตัดแต่งกระดูกอ่อน (Chondropasty) และการทำ OAT (Osteochodral Allograft Transfer) โดย
Gobbi และคณะ ศึกษาโดยการติดตามการรักษาและแบ่งกลุ่มแบบสุ่ม
(การวิจัยลำดับที่ II) พบว่าไม่มีความแตกต่างกันจาก Ankle-Hindfoot
Scale (AHS) และ Subjective Assessment Numeric Evaluation
(SANE)
จุดประสงค์ของการเจาะด้วยสว่านคือต้องการกระตุ้นไขกระดูกเช่นเดียวกับการทำเจาะผิวกระดูก
โดยความสำเร็จในการรักษามีรายงานดังนี้ Alexander และคณะพบว่า
ร้อยละ 89 (16 ใน 18คน) มีผลการรักษาที่ดีถึงดีมากเมื่อติดตามการรักษาเฉลี่ยถึง 58
เดือน อย่างไรก็ตาม Robinson และคณะพบว่าเพียง 31.8
เปอเซ็นต์ (7 ใน 22 คน) ที่มีอาการดีขึ้นเมื่อทำการรักษาด้วยการเจาะโดยใช้สว่าน
โดยมีคนไข้ 2 คนที่มีอาการปวดข้อเท้าหลังจากถูกเจาะด้วยสว่านอยู่
ภาพที่ 3 แสดงวิธีการทำเจาะผิวกระดูก (Microfracture)
(A)
แสดงตำแหน่งรอยโรคบริเวณส่วนหลางด้านในของกระดูกเทลัส
(B)
แสดงช่องทางในการส่องกล้องด้านหน้าโดย
1) ช่องทางด้านใน (Anteromedial) 2) ช่องทางด้านนอก
(Anterolateral) 3) ช่องทางเสริม (Accessory)
(C)
การทำความสะอาดรอยโรคที่ไม่มั่นคงโดยใช้
Shaver
ขนาด 4 มิลลิเมตร
(D)
– (E)
การทำการเจาะผิวกระดูกโดยใช้ Chondral Pick
(F) ภาพหลังจากการทำเจาะผิวกระดูก
(G) – (H)
หลังจากปลดสายห้ามเลือด มีเลือดออกจากบริเวณที่ทำการเจาะผิวกระดูก
การตัดกระดูก
ขูดกระดูก ร่วมกับการใช้กระดูกอ่อนจากเด็ก
กระดูกอ่อนบริจาคจากกระดูกอ่อนเด็ก
นำมาจากเด็กที่อายุน้อยกว่า 13 ปี DeNovo NT (Natural
Tissue) (Zimmer, Warsaw, IN) เป็นอุปกรณ์ทางการแพทย์ใหม่ที่ไม่มีร่างแห
โดยสามารถใส่ในส่วนที่ขาดหายไปและคลุมด้วนไฟบริน (Fibrin) โดยเทคนิคนี้สามารถที่จะทดแทนกระดูกอ่อนแบบไฮยาลิน
(Hyalin) โดยไม่ทำให้เกิดการบาดเจ็บบรเวณอื่นของผู้ป่วย โดยสามารถทำได้ทั้งการผ่าตัดแบบเปิดหรือการส่องกล้อง
เนื่องจากไม่จำเป็นต้องใช้พื้นที่ในการเข้าถึงเหมือนการนำเยื่อจากที่อื่น
หรือของบริจาคมาใช้ อย่างไรก็ตามในรอยโรคที่เข้าถึงได้ยาก
การตักกระดูกตาตุ่มด้านใน (Medial Malleolar Osteotomy) อาจจำเป็น
โดยมีวิธีการแสดงดังภาพที่ 4 ข้อบ่งชี้คือรอยโรคขนาดใหญ่
หรือรอยโรคที่ไม่ตอบสนองต่อการรักษาด้วยวิธีกระตุ้นไขกระดูก
โดยมีการศึกษามากมายในอดีตพบว่าวิธีรักษาดังกล่าวมีอาการดีขึ้นและปวดลดลงในกรณีที่ล้มเหลวกับการรักษาด้วยการกระตุ้นไขกระดูก
Coetzee
และคณะศึกษาหลังผ่าตัดข้อเท้า 24 ข้อพบ่วา ร้อยละ 78
ได้ผลการรักษาที่ดีถึงดีมาก โดยมี AOFAS เฉลี่ยที่ 85 คะแนน และมีคะแนนเฉลี่ย
FAAM สำหรับกิจกรรมและกีฬาที่ 82 และ 63 คะแนน
ร่วมกับคะแนนปวดดีขึ้น (VAS 24/100) โดยได้มีค่าเฉลี่ยติดตามการรักษาที่
16.2 เดือน โดยมีเนื้อเยื่อปลูกถ่ายเสื่อม 1 ราย
แต่ไม่พบภาวะแทรกซ้อนที่อันตรายนการศึกษาดังกล่าว
การผ่าตัดโดยการเจาะสว่านย้อนทาง
การผ่าตัดโดยเจาะสว่านย้อนทาง
(Retrograde
Drilling; RD) ใช้ในกรณีที่ผิวกระดูกอ่อนยังดีอยู่
โดยไม่ให้เกิดการบาดเจ็บต่อผิวกระดูกอ่อน มีการศึกษาในอดีตพบว่าอาการดีขึ้นทั้งในคนไข้เด็กและผู้ใหญ่
Taranow และคณะ ได้อธิบายวิธีผ่าตัดแบบนี้เป็นครั้งแรกในปี
ค.ศ.1999 โดยใช้การเข้าผ่าตัดทางด้านหน้า พบว่าคนไข้ทั้งหมด 16 คนมีคะแนน AOFAS
ก่อนผ่าตัดที่ 53.9 และหลังผ่าตัดเป็น 82.6
โดยติดตามไปถึง 25 เดือน ในขณะที่ Kono และคณะพบว่าการรักษาวิธีนี้มี
AOFAS 70.2 เพิ่มเป็น 96.8 เมื่อติดตามหลังผ่าตัดไปเป็นเวลา
2 ปี และ Ander และคณะ พบว่าอาการปวดดีขึ้นจาก 7.5/10 เป็น
3.7/10 เมื่อติดตามไปการรักษาไป 29 เดือน และมีการทำงานดีขึ้นจาก 4.6/10 เป็น
8.2/10
แต่วิธีการผ่าตัดนี้ต้องใช้ความสามารถอย่างมากเพื่อให้แม่ยำกับตำแหน่งรอยโรค
โดยพบโอกาสล้มเหลวถึง 20 เปอร์เซ็นต์ ซึ่งได้มีการเสนอวิธีใหม่ๆเพื่อเพอ่มความแม่นยำ
รวมทั้งลดเวลาในการผ่าตัดลง โดย Kermaa และคณะทำการศึกษาพบว่าการใช้ภาพถ่ายทางคลื่นแม่เหล็กไฟฟ้าพบว่า
มีความแม่นยำถึง 100 เปอร์เซ็นต์ ปลอดภัย พลิกแพลงได้ และไม่มีภาวะแทรกซ้อน และ Hoffmann
และคณะได้ใช้คลื่นแม่เหล็กไฟฟ้า (Electromagnetic Navigation
System) พบว่ามีความแม่นยำสูง และใช้เวลาผ่าตัดน้อยกว่าเมื่อทียบกับการใช้ภาพถ่ายรังสีในห้องผ่าตัด
และไม่นานมานี้ Ritcher และคณะได้เสนอการใช้ Navigated
Retrograde Drilling ในคนไข้ 52 คน พบว่า 48 คน มีอาการที่ดีขึ้น
(ค่าเฉลี่ยคะแนน SF-36 ได้ 96 คะแนน; ช่วงคะแนน
86-100 คะแนน
การผ่าตัดโดยการตัดกระดูกออก
ขูดกระดูกและนำกระดูกผู้ป่วยจากตำแหน่งอื่นมาใช้
เป้าหมายของการนำกระดูกผู้ป่วยมาถมในรอยโรคกระดูกอ่อนเทลัสบาดเจ็บที่มีช่องว่างคือเพื่อทำให้สามารถฟื้นฟูความสามารถในการรับน้ำหนักของกระดูกอ่อนได้
Bruns
กับคณะ และ Draper กับคณะ รายงานความสำเร็จในการรักษาด้วยวิธีนี้ถึง
85 เปอร์เซ็นต์ (28 ใน 33คน) Bruns และคณะ ศึกษาคนไข้ 26
คนในปี ค.ศ.1993 และรายงานว่าได้ผลดีถึงร้อยละ 70 และ Draper และคณะทำการศึกษาย้อนหลังเปรียบเทียบวิธีนี้ (14คน) กับการใช้สว่านเจาะ
(17คน) พบว่าการใช้วิธีนำกระดูกผู้ป่วยมาถมมีผลการรักษาที่ดีกว่าในด้านคะแนนรวม
การขยับของข้อเท้า อาการปวด และการเปรียบเทียบภาพถ่ายทางรังสี
โดยสรุปว่าการใช้กระดูกมาถมมีผลการรักษาในระยะยาวดีกว่าการรักษาด้วยวิธีการสว่านเจาะกระดูก
ภาพที่ 4 แสดงการใช้กระดูกอ่อนของเด็ก
(A), (B), (C) รอยโรคกระดูกอ่อนเทลัวบริเวณส่วนกลางด้านใน
(C) รอยโรคหลังจากการทำความสะอาด
(D) ใส่ Fibrin glue บริเวณฐานของรอยโรค
(E) การใส่กระดูกอ่อนของเด็ก
(F)
ใส่ Fibrin Glue คลุมกระดูกอ่อนอีกรอบ
การรักษาโดยการยึดชิ้นส่วนกระดูกอ่อนที่หลุดออกมา
ในอดีตมีงานศึกษารายงานถึงความสำเร็จในการยึดชิ้นส่วนกระดูกอ่อนขนาดใหญ่
รอยโรคส่วนใหญ่อยู่บริเวณด้านหน้าส่วนนอก โดยสัมพันธ์กับการบาดเจ็บ ซึ่งการตัดสินใจว่าจะยึดกระดูกอาจต้องดูว่าเป็นในคนไข้ที่อายุน้อย
มาในช่วงบาดเจ็บระยะแรก และชิ้นมีขนาดใหญ่เพียงพอ DeLee และคณะ แนะนำให้ยึดชิ้นกระดูกถ้ามีขนาดมากก่วา 1 ใน 3
ของส่วนผิวข้อของกระดูกเทลัส ในขณะที่ Stone และคณะ แนะนำให้ยึดเมื่อขนาดชิ้นใหญ่มากกว่า
7.5 มิลลิเมตร งานวิจัยของ Kumai และคณะ ซึ่งเป็นงานวิจัยที่มีจำนวนผู้ป่วยมากที่สุด
(27คน) ได้มีค่าเฉลี่ยการติดตาม 7 ปี พบว่าได้ผลการรักษาที่ดีร้อยละ 89 (24 ใน
27คน) และ ในปี ค.ศ.2008 Chandran และคณะ
รายงายผลการรักษาที่ดีเยี่ยมโดยใช้ หมุดที่สลายได้ (Absorbable Pin) Schepers และคณะ รายงานถึงความสำเร็จในการใช้
หมุดที่สลายได้ในปี ค.ศ.2011 รวมทั้ง Kim และคณะ
รายงานความสำเร็จในการรักษารอยโรคตำแหน่งด้านหลังส่วนในโดยใช้การส่องกล้องทางด้านหลัง
การรักษาโดยใชการนำเซลล์กระดูกอ่อนไปเพาะเลี้ยงและนำมาใช้
(Autologous Chondrocyte Implantation; ACI)
การรักษาโดยใชการนำเซลล์กระดูกอ่อนไปเพาะเลี้ยงและนำมาใช้
โดยคลุมด้วยแผ่นเยื่อหุ้มกระดูก (Periosteal Patch) เซลล์กระดูกอ่อนสามารถเอามาจากชิ้นส่วนกระดูกอ่อนที่หลุด
ขอบของรอยโรค หรือจากข้อเข่า โดยรอยโรคของกระดูกอ่อนต้องได้รับการทำความสะอาดจนไม่มีเนื้อเยื่อที่ตายและขอบมั่นคง
โดยจะนำการเก็บเกี่ยวโดยใช้ประมาณ 200-300 มิลลิกรัม และนำไปเพะเลี้ยงอีก 6-8
สัปดาห์ จนได้เป็น 12 ล้านเซลล์ ซึ่งเพิ่มขึ้นประมาณ 10 เท่า จากนั้นจึงทำแม่พิมพ์ขนาดของรอยโรคและนำไปใช้กับเยื่อหุ้มกระดูกของกระดูกขาส่วนล่าง
โดยนำเยื่อหุ้มกระดูกเย็บปิด คลุมด้วยไฟบริน จากนั้นจึงฉีดเซลล์ที่เพาะเลี้ยงเข้าไป
ข้อบ่งชี้คือเป็นรอยโรคที่เป็นหลุมที่มีขนาดมากกว่า 1.0-1.5 ตารางเซนติเมตร
มีงานศึกษาก่อนหน้านี้รายงานถึงความสำเร็จในการรักษาโดยใช้
เทคนิค ACI
โดยมีคะแนนเฉลี่ย AOFAS เพิ่มขึ้นจาก 25.2 เป็น
45.0 Whittaker และคณะ ศึกษาคนไข้ 9 รายโดยติดตามไปประมาณ 23
เดือนพบว่ามีค่า คะแนน Mazur ของข้อเท้าดีขึ้น 23 คะแนนและมีผลกระทบบริเวณตำแหน่งที่เอามาเพียงเล็กน้อย
โดยรอยโรคสามารถเก็บได้เรียบและได้กระดูกอ่อนที่มั่นคง
เมื่อนำชิ้นเนื้อมาตรวจพบว่า ได้กระดูกอ่อนแบบ Fibrocartilage ร่วมกับ Hyalin Cartilage เล็กน้อย รวมั้ง Baums
และคณะศึกษาผู้ป่วย 12 รายโดยติดตามไปประมาณ 63 เดือน พบว่าคะแนน AOFAS
ดีขึ้นจาก 43.5 เป็น 88.5 คะแนน และคะแนน Hannover ดีขึ้นจาก 40.4 เป็น 85.5 คะแนน Giannini และคณะทำ ACI
ในผู้ป่วย 46 ราย โดยติดตามไปประมาณ 18 เดือน พบว่าคะแนน AOFAS
ดีขึ้นจากก่อนผ่าตัด 57.2 คะแนน และหลังผ่าตัด 36 เดือน เป็น 89.5
คะแนน และเมื่อไม่นานมานี้ matrix associated ACI (MACI) ได้นำมาใช้แทนการใช้
เยื่อหุ้มกระดูก (Periosteal Flap) ทำให้ทำได้ง่ายขึ้นและประหยัดเวลามากขึ้น
Ander และคณะ รายงานการใช้ MACI ในผู้ป่วย
22 ราย โดยติดตามไปประมาณ 63.5 เดือน พบว่าเทคนิดดังกล่าวเพิ่มคะแนน AOFAS ได้อย่างมีนัยสำคัญจาก 70.1 เป็น 95.3 คะแนน คะแนนปวด (VAS) จาก 5.7/10 เป็น 0.9/10 และ Tegner activity level เพิ่มจาก
2.4 เป็น 4.7 ที่ 60 เดือนหลังผ่าตัดโดยไม่มีภาวะแทรกซ้อนรุนแรง จากที่กล่าวมา ACI
ดูเป็นทางเลือกในการรักษาที่ได้ผลที่ค่อยข้างดีอย่างไรก็ตามยังคงมีปัญหาบริเวณที่เก็บเกี่ยว
(Donor site Morbidity) และราคาสูง
การเคลื่อนย้ายกระดูกอ่อนจากที่อื่น
(Osteochondral
Autograft Transportation)
วิธีนี้เป็นการนำกระดูกอ่อนจากบริเวณที่ลงน้ำหนักน้อย
เช่น บริเวณเข่า หรือบริเวณกระดูกเทลัสเอง โดยเป้าหมายเพื่อฟื้นฟูหน้าที่ที่สำคัญของกระดูกอ่อน
Hyaline ทั้งด้าน กายภาพ ชีวเคมี และกลศาสตร์
ข้อบ่งชี้คือรอยโรคที่มีขนาดใหญ่ (มากกว่า 10-15 มิลลิเมตร)
หรือหลังจากการรักษาด้วยวิธีที่กล่าวไปข้างต้นแล้วล้มเหลว
โดยวิธีนี้สามารถทำได้ทั้งแบบ Mosaicplasty หรือ Osteochondral
Autograft Transplantation (OATS)
การเคลื่อนย้ายกระดูกอ่อนพบว่าเป็นวิธีที่มีความสำเร็จโดยมีคะแนน
AOFAS
เพิ่ม 5.7 ถึง 27 คะแนน Hangody และคณะ
ศึกษาผู้ป่วย 11 รายที่ได้รับการทำ Mosaicplasty ในปี 1997
โดยได้ผลดีร้อยละ 82 จากคะแนน Hannover Ankle/Bandi Knee Morbidity และ Scranton และคณะ รายงานว่า ผู้ป่วยร้อยละ 90 (45
ใน 90คน) ได้ผลดีถึงดีเยี่ยม รวมทั้งมีความพึงพอใจ เมื่อติดตามหลังผ่าตัดไป 36
เดือน รวมทั้ง Sammarco และคณะ รายงานผู้ป่วย 12 ราย โดยใช้เนื้อเยื่อจากกระดูกเทลัสข้างเดียวกัน
พบว่าคะแนน AOFAS ดีขึ้นจาก 64.4 เป็น 90.8 คะแนนหลังติดตามไปได้ประมาณ
25.3 เดือน
แม้ว่ารายงานก่อนหน้าได้ชี้ว่าการรักษาวิธีนี้ได้ผลดี
แต่อย่างไรก็ตาม วิธีดังกล่าวเป็นการทำให้กระดูกอ่อนที่ปกติถูกรบกวน
ซึ่งอาจส่งผลให้เกิดปัญหา โดยพบว่ามีปัญหาปวดเข่าตามมาได้ถึง 5-50 เปอร์เซ็นต์
ในขณะเดียวกัน Reddy และคณะ รายงานว่า ร้อยละ 36
ของผู้ป่วย (4 ใน 11 คน) มีอาการที่เข่าแย่โดยวัดจาก Lysholm ซึ่งภาวะแทรกซ้อนเหล่านี้ควรต้องอธิบายผู้ป่วยก่อนที่จะเลือกการรักษาด้วยวิธีดังกล่าว
การเคลื่อนย้ายปลูกถ่ายกระดูกจากผู้บริจาค
(Osteochondral
Allograft Transplantation)
การเคลื่อนย้ายปลูกถ่ายกระดูกจากผู้บริจาคเป็นวิธีที่ได้ผลดีในการรักษารอยโรคที่ใหญ่
โดยได้รูปร่างผิวกระดูกอ่อนที่สามารถช่วยรับน้ำหนักกับกระดูกอ่อนปกติที่เหลือ
ซึ่งสามารถช่วยป้องกันภาวะข้อเสื่อมในอนาคตได้ โดยวิธีนี้จะไม่ทำให้เกิดผลกระทบจากบริเวณที่อื่นของผู้ป่วย
รวมทั้งสามารถใช้เป็นเนื้อกระดูกชิ้นเดียวทำให้มีการเกิดของกระดูกอ่อน
Fibrocartilage ได้น้อยเมื่อเทียบกับการทำแบบ Mosaiplasty วิธีนี้ได้แสดงดังรูปที่ 5 ข้อบ่งชี้คือรอบโรคที่ใหญ่และลึก
รวมทั้งล้มเหลวในการผ่าตัดก่อนหน้า
งานศึกษาก่อนหน้ารายงานว่า
วิธีนี้ทำให้การทำงานของเท้าและข้อเท้าดีขึ้น Berlet และคณะ
ได้ทำการนำกระดูกผู้บริจาคสด 19 ราย โดยติดตามเฉลี่ย 3.3 ปี พบว่ามีคะแนน AOFAS
ดีขึ้นจากก่อนผ่าตัด 61 เป็น หลังผ่าตัด 79 คะแนน
อย่างไรก็ตามไม่พบการดีขึ้นของ SF-36 PCD และ คะแนน MCS
subscale ในขณะเดียวกัน El-Rashidy และคณะ
รายงานศึกษาผู้ป่วย 42 รายโดยติดตามไป 37.7 เดือน โดยมีคะแนน AOFAS และ VAS ดีขึ้น จาก 52 เป็น 79 และ 8.2 เป็น 3.3
คะแนนตามลำดับ โดยพวกเขายังได้รายงานอีกว่าเนื้อเยื่อที่นำมา มั่นคง เนียน
และมีการยุบเพียงเล็กน้อยเมื่อติดตามด้วย MRI หลังผ่าตัด และ
Adams และคณะ รายงานจากการติดตามไประยะกลาง 48 เดือน พบว่าอาการปวดดีขึ้น
(VAS จาก 6/10 เป็น 1/10) และ ค่าเฉลี่ย AOFAS เป็น 84 คะแนน เมื่อทำการติดตามภาพถ่ายทางรังสีพบว่าผู้ป่วย 5 รายมีรอยไม่เชื่อติด
อย่างไรก็ตามไม่มีเนื้อเยื่อใดที่ล้มเหลว รวมทั้ง Raikin และคณะรายงานศึกษาผู้ป่วย
15 ราย พบว่า AOFAS ดีขึ้นจาก 38 เป็น 83 คะแนน และ VAS
จาก 8.5/10 เป็น 3.3/10 ที่ติดตามหลังผ่าตัด 54 เดือน โดยไม่พบว่าแทรกซ้อน
อย่างไรก็ตามภาพถ่ายทางรังสีมีภาวะยุบและเนื้อเยื่อสลายใน 10 จาก 15 ข้อเท้า และ 9
ข้อเท้ามีภาวะข้อที่แคบลงในบริเวณเนื้อเยื่อที่ปลูกถ่ายมา
ภาพที่
5 แสดงการเคลื่อนย้ายปลูกถ่ายกระดูกผู้บริจาค
(A)
การตัดกระดูกตาตุ่มในเพื่อใช้ในการเข้าถูกรอยโรคที่ใหญ่บริเวณส่วนกลางด้านใน
(MM
= กระดูกตาตุ่มใน)
(B)
การวัดรอยโรคโดยใช้อุปกรณ์วัด
และใช้ K-wire
ใส่บริเวณตำแหน่งตรงกลางของรอยโรค
(C)
การเตรียมผิวกระดูก
ให้ได้ความลึก 6-8 มิลลิเมตร
(D)
วัดระดับความลึกของรอยโรค
(E)
การนำกระดูกเทลัสผู้บริจาคมาใช้
(F) หลังจากนำกระดูกเทลัสมาปลูกถ่าย
การใช้โลหะแทนที่
(Metal
Inlay Implant)
มีการใช้โลหะ
(Hemicap, Arthrosurface, Frankin, MA) รายงานในปี ค.ศ.2007
ในรอยโรคด้านตาตุ่มในขอเทลัส จุดประสงค์ของการใช้อุปกรณ์โลหะนี้ช่วยลดปวดและป้องกันการเกิดถุงน้ำในกระดูก
วิธีนี้ต้องใช้ความแม่นยำในการผ่าตัดเพราะสามรถบาดเจ็บต่ออวันวะข้างเคียง เช่น
บริเวณข้อของกระดูกขาส่วนล่าง หรือถ้าลึกมากไปก็อาจจะทำให้กระดูกอ่อนและกระดูกข้างใต้ยุบได้
ข้อบ่งชี้คือ ผู้ป่วยที่มีรอยโรคบริเวณ Medial Talar Dome ที่มีขนาดใหญ่และล้มเหลวในการผ่าตัดครั้งแรก
ใบปัจจุบันมีงานวิจัยศึกษาเพียงเล็กน้อย
ข้อมูลปัจจุบันที่เป็นการศึกษาไปข้างหน้าของ van Bergen และคณะ ศึกษาผู้ป่วย 20 ราย โดยรายงานว่าคะแนน AOFAS ดีขึ้นจาก 62 เป็น 87 และ SF-36 (PCS subscale) จาก
36 เป็น 45 คะแนนหลังติดตามไปประมาณ 3 ปี โดยไม่พบการดีขึ้นของ SF-36 (MCS
subscale)
สรุป
·
สาเหตุและกลไลการเกิดโรคกระดูกอ่อนบาดเจ็บของเทลัสยังไม่มีข้อสรุป
อย่างไรก็ตามคาดว่าสัมพันธ์กับข้อเท้าบาดเจ็บ และ การที่ข้อเท้าไม่มั่นคง
·
การรักษาในปัจจุบันยังไม่มีข้อสรุป
โดยในกรณีชิ้นส่วนกระดูกที่ยังไม่หลุดเคลื่อน Berdt และ
Harty ขั้น I และ II ควรรักษาด้วยการรักษาแบบไม่ผ่าตัด ด้วยการใส่เฝือกและจำกัดกิจกรรม
ซึ่งถ้ารักษาไม่ประสบความสำเร็จ อาจเป้นข้อบ่งชี้ในการรักษาโดยการผ่าตัด
·
ในกรณีที่บาดเจ็บฉับพลัน
และกระดูกเคลื่อนหลุดที่ขนาดใหญ่กว่า 7.5 มิลลิเมตร หรือใหญ่กว่า 1 ใน 3
ของผิวหน้ากระดูกเทลัส ในคนไข้หนุ่ม
สามารถสำเร็จได้โดยการรักษาด้วยการผ่าตัดแบบเปิดและยึดตรึงกระดูก
·
ถ้าขนาดของรอยโรคเล็กกว่า
15 มิลลิเมตร และ ลึกน้อยกว่า 7 มิลลิเมตร การรักษาโดยการกระตุ้นไขกระดูก
โดยใช้วิธี ตัดส่วนที่บาดเจ็บออก ขูดกระดูก และเจาะกระดูก โดยสามารถทำได้ทั้งการส่องกล้องทั้งทางด้านหน้า
หรือทางด้านหลัง อย่างไรก็ตามการกระตุ้นไขกระดูกพบว่าเป็นวิธีที่มีความสำเร็จในการรักษารอยโรคขนาดเล็ก
โดยเนื้อเยื่อที่ทำการรักษาจะเป็นกระดูกอ่อนแบบ Fibrocartilage
(Type I Collagen เป็นส่วนมาก)
ซึ่งมีความคงทนน้อยกว่า Hyaline Cartilage (Type II Collagen เป็นส่วนมาก)
·
ถ้าขนาดของรอยโรคใหญ่และลึก
หรือล้มเหลวจากการรักษาด้วยการกระตุ้นไขกระดูก มีงานวิจัยที่สนับสนุนการใช้
กระดูกอ่อนเด็ก การใช้เซลล์กระดูกอ่อนไปเพาะเลี้ยง การเคลื่อนถ่ายกระดูกของตัวผู้ป่วยเอง
การปลูกถ่ายกระดูกของผู้บริจาค อย่างไรก็ตามการใช้โดยการเคลื่อนถ่ายกระดูกของตัวผู้ป่วยเอง
อาจต้องคลำนึงถึงภาวะแทรกซ้อนจากบริเวณที่เอากระดูกมา